아주대 김용성 교수, 세포 내 종양유발 단백질 표적 기술 개발
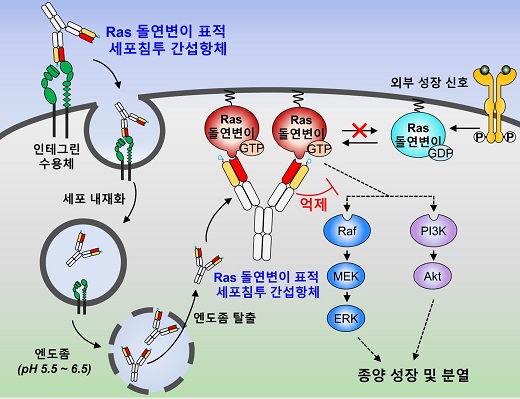
라스 표적 세포침투 간섭항체의 원리.한국연구재단 제공
한국연구재단(이사장 조무제)은 아주대 김용성 교수팀이 암유발 단백질 라스(Ras) 돌연변이를 직접 표적해 종양의 성장을 막는 치료용 항체 기술을 개발했다고 22일 밝혔다.
라스 돌연변이 단백질은 종양의 약 30%에서 발견되는 가장 널리 알려진 종양유발 인자다.
이 단백질은 췌장암에서 약 95%, 대장암에서 약 52%, 비소세포폐암에서는 약 30%로 발견된다.
지난 1982년 최초 발견된 이후 라스 돌연변이를 직접 표적하는 약물이 개발되지 않아 ‘난공불락 표적’으로 여겨졌다.
지금까지의 항체 치료제는 세포막을 투과해 세포질로 침투할 수 없어 질환유발 단백질을 직접 표적할 수 없는 한계가 있다.
연구팀은 활성화된 라스 돌연변이에 특이적으로 결합, 활성을 저해하는 세포침투 간섭항체를 제조했다.
이 간섭항체는 종양세포 표면에 과발현돼 있는 ‘인테그린 수용체’와 결합해 세포에 내재화 된 후에 엔도좀 탈출(세포 내 막주머니인 엔도좀에서 세포질로 나오는 과정)로 세포질 안에 들어가 라스 돌연변이와 결합한다.
연구팀은 이 항체를 세포 및 동물시험 연구에 적용해 대장암, 육종암의 암세포 증식을 억제하는 결과를 얻었다.
연구팀은 이 기술은 기존 항체가 표적하지 못했던 세포질 내의 질환관련 단백질을 항체로 직접 표적하는 플랫폼이 될 것으로 기대하고 있다.
또한 향후 임상시험 단계를 거쳐 제품화로 이어지면 연간 900억 달러(2016년 기준)에 달하는 국·내외 치료용 항체 시장에 진출할 수 있을 것으로 전망하고 있다.
김용성 교수는 “필요성이 크지만 현재까지 약물이 없었던 라스 돌연변이 단백질을 직접 표적하는 신약 항체 치료제 개발의 가능성을 열었다고 생각한다”고 말했다.
이번 연구결과는 국제학술지 네이처 커뮤니케이션즈(Nature Communications) 5월10일 자에 게재됐다.
ynwa21@ilyodsc.com